Die Fluoreszenzmikroskopie ist eine unverzichtbare Technik in vielen wissenschaftlichen Disziplinen, insbesondere in der Biologie und Medizin. Sie ermöglicht die Visualisierung spezifischer Strukturen oder Moleküle innerhalb von Zellen und Geweben mit hoher Sensitivität. Im Kern dieser Technik steht das Phänomen der Fluoreszenz, bei dem spezielle Farbstoffe, sogenannte Fluorochrome, eine entscheidende Rolle spielen. Diese Moleküle besitzen die faszinierende Fähigkeit, Licht einer bestimmten Wellenlänge zu absorbieren und diese Energie dann als Licht einer längeren Wellenlänge wieder abzugeben. Das Verständnis der beteiligten Wellenlängen und Prozesse ist fundamental, um optimale Fluoreszenzbilder zu erzielen.
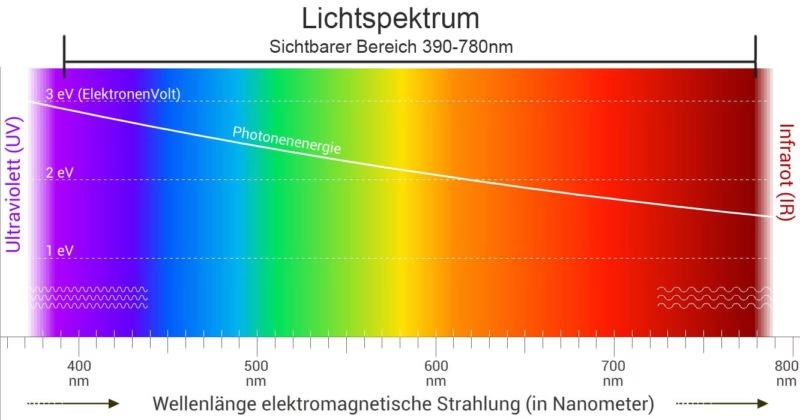
Grundlagen der Fluoreszenzanregung und -emission
Fluorochrome sind chemische Verbindungen, die auf Licht reagieren. Wenn sie mit Licht einer geeigneten Energie (und damit Wellenlänge) bestrahlt werden, nehmen sie Photonen auf und gelangen in einen angeregten Energiezustand. Dieser Prozess wird als Anregung bezeichnet und erfolgt bei einer spezifischen Wellenlänge oder einem Bereich von Wellenlängen, die für das jeweilige Fluorochrom charakteristisch sind. Nach einer sehr kurzen Verweildauer im angeregten Zustand kehren die Fluorochrome in ihren Grundzustand zurück und geben dabei die zuvor aufgenommene Energie teilweise als Licht wieder ab. Dieses emittierte Licht hat eine geringere Energie und somit eine längere Wellenlänge als das anregende Licht. Diesen Vorgang nennt man Fluoreszenzemission.
Die Effizienz dieses Prozesses, also wie gut ein Fluorochrom Licht absorbiert und wie viel davon als Fluoreszenz wieder abgegeben wird, ist von verschiedenen Faktoren abhängig und wird durch charakteristische Spektren beschrieben.
Charakteristische Spektren: Anregung und Emission
Jedes Fluorochrom hat ein einzigartiges Paar von Spektren: ein Absorptions- (oder Anregungs-) Spektrum und ein Emissionsspektrum. Diese Spektren stellen die relative Intensität der Absorption oder Emission über einen Bereich von Wellenlängen dar. Typischerweise wird die relative Intensität auf der vertikalen Achse und die Wellenlänge auf der horizontalen Achse aufgetragen.
Bestimmung des Emissionsspektrums
Um das Emissionsspektrum eines Fluorochroms zu bestimmen, wird das Fluorochrom bei der Wellenlänge seiner maximalen Absorption angeregt. Anschließend wird die Intensität des emittierten Fluoreszenzlichts über einen breiten Wellenlängenbereich gemessen. Dies geschieht oft mit einem Monochromator, einem Gerät, das nur Licht schmaler Wellenlängenbänder durchlässt. Durch das Durchsuchen verschiedener Wellenlängen und die Messung der jeweiligen Fluoreszenzintensität entsteht das Emissionsspektrum.
Bestimmung des Anregungsspektrums
Ähnlich wird das Anregungsspektrum ermittelt. Hierbei wird die Fluoreszenzemission bei einer festen Wellenlänge, typischerweise der Wellenlänge der maximalen Emission, gemessen. Das Fluorochrom wird dann nacheinander mit Licht verschiedener Anregungswellenlängen bestrahlt (z. B. ebenfalls mithilfe eines Monochromators). Die gemessene Intensität der Fluoreszenz bei der festen Emissionswellenlänge, aufgetragen gegen die jeweilige Anregungswellenlänge, ergibt das Anregungsspektrum. Für reine Verbindungen ähneln sich Absorptions- und Anregungsspektren oft sehr.
Das Stokes-Gesetz
Ein fundamentales Prinzip in der Fluoreszenz ist das Stokes-Gesetz, benannt nach Sir George G. Stokes. Es besagt, dass das emittierte Fluoreszenzlicht immer eine längere Wellenlänge aufweist als das anregende Licht. Dies ist darauf zurückzuführen, dass bei der Rückkehr des Elektrons vom angeregten Zustand in den Grundzustand Energie in Form von Wärme durch Schwingungsrelaxation verloren geht, bevor das Photon emittiert wird. Da die Wellenlänge umgekehrt proportional zur Energie ist, führt dieser Energieverlust zu einer Verschiebung des Emissionsspektrums zu längeren Wellenlängen im Vergleich zum Anregungsspektrum. Je größer diese Stokes-Verschiebung ist, desto einfacher ist es, das helle Anregungslicht vom schwächeren emittierten Fluoreszenzlicht zu trennen.
Trennung der Wellenlängen: Die Rolle der Filter
Ein wichtiger Aspekt bei der Fluoreszenzmikroskopie ist die notwendige Trennung des Anregungslichts vom Emissionslicht. Anhand typischer Spektren ist ersichtlich, dass es in der Regel eine gewisse Überlappung zwischen dem Anregungsspektrum (am längerwelligen Ende) und dem Emissionsspektrum (am kürzerwelligen Ende) gibt. Da das Anregungslicht in der Regel viel heller ist als das emittierte Fluoreszenzlicht, würde diese Überlappung den Kontrast des Fluoreszenzbildes erheblich reduzieren oder die schwache Fluoreszenz komplett überstrahlen.
Um dies zu verhindern, werden spezielle optische Filter eingesetzt. In einem typischen Fluoreszenzmikroskop werden Anregungsfilter, Emissionsfilter und ein Strahlteiler (oft ein dichroitischer Spiegel) in einem sogenannten Filterwürfel kombiniert. Der Anregungsfilter lässt nur die gewünschten Wellenlängen des Anregungslichts zur Probe durch. Der Strahlteiler lenkt das Anregungslicht auf die Probe. Das von der Probe emittierte Fluoreszenzlicht, das nun längere Wellenlängen hat, passiert den Strahlteiler und gelangt zum Emissionsfilter. Der Emissionsfilter lässt nur das emittierte Fluoreszenzlicht passieren und blockiert verbleibendes Anregungslicht sowie Streulicht. Diese sorgfältige Filterauswahl ist entscheidend, um ein klares und kontrastreiches Fluoreszenzbild zu erhalten.
Effizienz der Fluoreszenz
Die Intensität der Fluoreszenzemission, die wir beobachten, hängt von mehreren Faktoren ab, die die Effizienz des Fluoreszenzprozesses bestimmen:
- Molekularer Extinktionskoeffizient: Dieses Maß beschreibt, wie effizient ein Fluorochrom das Anregungslicht bei einer bestimmten Wellenlänge absorbiert. Ein höherer Extinktionskoeffizient bedeutet eine stärkere Absorption und damit eine größere Wahrscheinlichkeit für Fluoreszenz.
- Quantenausbeute: Die Quantenausbeute ist das Verhältnis der Anzahl emittierter Photonen zur Anzahl absorbierter Photonen. Sie gibt an, wie effizient das absorbierte Licht in Fluoreszenz umgewandelt wird. Werte liegen typischerweise zwischen 0 und 1. Eine Quantenausbeute von 1 bedeutet, dass jedes absorbierte Photon zur Emission eines Fluoreszenzphotons führt. Werte unter 1 deuten auf Energieverlust durch andere Prozesse (z. B. Wärme, chemische Reaktionen) hin.
Hier ist eine Tabelle mit Quantenausbeuten für einige ausgewählte Fluorochrome:
| Chemische Verbindung | Lösungsmittel | Anregung Wellenlänge (nm) | Emission Wellenlänge (nm) | Quantenausbeute |
|---|---|---|---|---|
| Acridinorange | Ethanol | 493 | 535 | 0,46 |
| Benzol | Ethanol | 248 | 300-350 | 0,04 |
| Chlorophyll-A | Ethanol | 440 | 685 | 0,23 |
| Eosin | Wasser | 521 | 544 | 0,16 |
| Fluorescein | Wasser | 437 | 515 | 0,92 |
| Rhodamin-B | Ethanol | 555 | 627 | 0,97 |
Neben diesen intrinsischen Eigenschaften des Fluorochroms beeinflussen auch externe Faktoren die Fluoreszenzintensität. Dazu gehören die Helligkeit der Lichtquelle, die Fluoreszenzlebensdauer (die Verweildauer im angeregten Zustand) und die chemische Umgebung des Fluorochroms. Variablen wie die Viskosität des Lösungsmittels, die Ionenkonzentration, der pH-Wert und die Hydrophobie der Umgebung können die Fluoreszenz stark beeinflussen.
Molekulare Mechanismen: Das Jablonski-Diagramm
Der Fluoreszenzprozess auf molekularer Ebene kann mithilfe eines Jablonski-Diagramms visualisiert werden. Dieses Diagramm zeigt die Energiezustände eines Moleküls und die Übergänge zwischen ihnen:
- Grundzustand (S0): Im Ruhezustand befinden sich die Elektronen im niedrigsten Energiezustand.
- Absorption: Das Molekül absorbiert ein Photon des Anregungslichts und ein Elektron springt in einen höheren elektronischen Anregungszustand (z. B. S1, S2,...). Innerhalb dieser elektronischen Zustände gibt es auch verschiedene Schwingungsunterzustände. Die Anregung führt typischerweise in einen höheren Schwingungsunterzustand eines angeregten Zustands. Dieser Schritt dauert nur wenige Femtosekunden (10^-15 Sekunden).
- Schwingungsrelaxation (Internal Conversion): Das angeregte Elektron gibt schnell (innerhalb von Pikosekunden, 10^-12 Sekunden) Schwingungsenergie an die Umgebung ab und fällt auf den niedrigsten Schwingungsunterzustand des niedrigsten angeregten Singulett-Zustands (S1) zurück. Hierbei geht Energie verloren, was zur Stokes-Verschiebung führt.
- Fluoreszenzemission: Vom niedrigsten Schwingungsunterzustand des S1-Zustands fällt das Elektron unter Emission eines Fluoreszenzphotons zurück in einen Schwingungsunterzustand des Grundzustands (S0). Dieses emittierte Licht hat eine längere Wellenlänge als das Anregungslicht. Dieser Prozess dauert typischerweise Nanosekunden (10^-9 Sekunden). Die Fluoreszenz hört auf, sobald die Anregungslichtquelle abgeschaltet wird.
Neben der Fluoreszenz gibt es auch andere mögliche Übergänge:
- Intersystem Crossing: Gelegentlich kann das Elektron vom Singulett-Zustand (S1) in einen energetisch niedrigeren, aber spin-verbotenen Triplett-Zustand (T1) wechseln.
- Phosphoreszenz: Vom Triplett-Zustand (T1) kann das Elektron mit verzögerter Emission (oft Millisekunden bis Sekunden) in den Grundzustand zurückfallen. Dies ist Phosphoreszenz.
- Verzögerte Fluoreszenz: In manchen Fällen kann ein Elektron vom Triplett-Zustand (T1) zurück in den Singulett-Zustand (S1) gelangen und von dort Fluoreszenz emittieren. Dieser Prozess dauert länger als normale Fluoreszenz (Mikrosekunden).
Probleme: Photobleaching und Quenching
Unter bestimmten Bedingungen kann die Fluoreszenzintensität im Laufe der Zeit abnehmen. Dieses Phänomen wird als Verblassen oder Photobleaching bezeichnet. Photobleaching ist eine irreversible Zerstörung des Fluorochroms, oft verursacht durch chemische Reaktionen (z. B. Oxidation durch molekularen Sauerstoff) im angeregten Zustand unter Lichteinwirkung. Je intensiver das Anregungslicht und je länger die Belichtungszeit, desto schneller tritt Photobleaching auf.
Ein verwandtes Phänomen ist das Quenching. Quenching führt ebenfalls zu einer verminderten Fluoreszenzintensität, ist aber oft reversibel und wird durch die Interaktion des angeregten Fluorochroms mit anderen Molekülen in seiner Umgebung verursacht. Beispiele hierfür sind die Kollision mit Sauerstoffmolekülen oder das Vorhandensein von Schwermetallsalzen oder Halogenverbindungen. Eine Form des Quenchings ist der Resonanzenergietransfer (Förster Resonance Energy Transfer, FRET), bei dem Energie von einem angeregten Fluorochrom (Donor) strahlungsfrei auf ein nahegelegenes Akzeptormolekül übertragen wird, wenn sich deren Spektren überlappen.
Photobleaching kann auch gezielt eingesetzt werden, zum Beispiel bei der Technik FRAP (Fluorescence Recovery After Photobleaching). Hierbei wird ein Bereich der Probe durch einen kurzen, intensiven Laserpuls gezielt ausgebleicht, um anschließend die Dynamik (z. B. Diffusion) nicht ausgebleichter Fluorochrome in diesen Bereich zu verfolgen.
Schutz vor Ausbleichen (Antifade)
Um das Ausmaß des Photobleachings zu reduzieren und die Beobachtungszeit zu verlängern, können verschiedene Maßnahmen ergriffen werden:
- Reduzierung der Anregungslichtintensität: Durch die Verwendung von Neutraldichtefiltern im Anregungsstrahlengang kann die Lichtintensität reduziert werden, was das Ausbleichen verlangsamt, allerdings auch die Emissionsintensität verringert.
- Anpassung des Mediums: Eine Änderung des pH-Werts des Mediums kann in manchen Fällen helfen.
- Verwendung von Antifade-Reagenzien: Diese chemischen Zusätze im Einbettungsmedium oder der Probenlösung können das Ausbleichen signifikant reduzieren. Sie wirken oft als Antioxidantien, die reaktive Sauerstoffspezies abfangen, welche am Photobleaching beteiligt sind.
Hier sind einige gängige Antifade-Reagenzien:
| Antifade-Reagenz | Beschreibung |
|---|---|
| p-Phenylendiamin | Sehr effektiv für FITC und Rhodamin. Wird oft in Glycerin/PBS verwendet. Muss lichtgeschützt gelagert werden und ist giftig. |
| DABCO (1,4-Diazabicyclo-2,2,2-octan) | Effektiv für FITC. Etwas weniger wirksam als p-Phenylendiamin, aber lichtbeständiger und sicherer. |
| n-Propylgallat | Sehr effektiv für Rhodamin, auch für FITC. Wird oft in Glycerin/PBS verwendet. |
| 2-Mercaptoethylamin | Nützlich für Proben, die mit Propidiumjodid, Acridinorange oder Chromomycin A3 gefärbt sind, z. B. Chromosomen. Wird oft in Tris-EDTA verwendet. |
Zusätzlich zu chemischen Methoden kann auch eine schnelle Bildaufnahme oder ein rascher Wechsel des Sichtfelds dazu beitragen, die Belichtung der Probe zu minimieren und so das Ausbleichen zu verringern.
Häufig gestellte Fragen (FAQs)
Was ist der Unterschied zwischen Anregungs- und Emissionswellenlänge?
Die Anregungswellenlänge ist die Wellenlänge des Lichts, das vom Fluorochrom absorbiert wird, um es in einen angeregten Zustand zu bringen. Die Emissionswellenlänge ist die längere Wellenlänge des Lichts, das vom Fluorochrom emittiert wird, wenn es in seinen Grundzustand zurückkehrt.
Was erklärt das Stokes-Gesetz?
Das Stokes-Gesetz erklärt, dass das emittierte Fluoreszenzlicht immer eine längere Wellenlänge hat als das anregende Licht. Dies liegt am Energieverlust durch Schwingungsrelaxation im angeregten Zustand.
Warum sind Filter in der Fluoreszenzmikroskopie so wichtig?
Filter sind entscheidend, um das viel hellere Anregungslicht vom schwächeren emittierten Fluoreszenzlicht zu trennen. Sie stellen sicher, dass nur das Fluoreszenzsignal den Detektor erreicht und ein klares, kontrastreiches Bild entsteht.
Was ist die Quantenausbeute eines Fluorochroms?
Die Quantenausbeute ist ein Maß für die Effizienz der Fluoreszenz. Sie gibt das Verhältnis der Anzahl emittierter Photonen zur Anzahl absorbierter Photonen an. Eine hohe Quantenausbeute bedeutet, dass viel vom absorbierten Licht als Fluoreszenz reemittiert wird.
Was versteht man unter Photobleaching?
Photobleaching ist die irreversible Zerstörung von Fluorochromen durch Lichteinwirkung, oft durch chemische Reaktionen im angeregten Zustand. Es führt zu einer Abnahme der Fluoreszenzintensität über die Zeit.
Wie kann man Photobleaching in Proben reduzieren?
Photobleaching kann durch Reduzierung der Anregungslichtintensität, Anpassung der chemischen Umgebung (z. B. pH-Wert) oder Zugabe von Antifade-Reagenzien zum Medium verringert werden.
Fazit
Die Wellenlängen der Anregung und Emission sind fundamentale Eigenschaften von Fluorochromen und bestimmen maßgeblich, wie Fluoreszenz in der Mikroskopie genutzt werden kann. Das Zusammenspiel von spezifischen Spektren, dem Stokes-Gesetz, der sorgfältigen Auswahl optischer Filter und dem Verständnis von Effizienzfaktoren wie Extinktionskoeffizient und Quantenausbeute ist entscheidend für die Erzielung qualitativ hochwertiger Fluoreszenzbilder. Darüber hinaus erfordern Herausforderungen wie Photobleaching und Quenching spezifische Strategien und Reagenzien, um die Fluoreszenzsignale während der Bildgebung zu erhalten. Ein tiefes Verständnis dieser Prinzipien ermöglicht es Forschern und Fotografen, das volle Potenzial der Fluoreszenzmikroskopie auszuschöpfen und faszinierende Einblicke in die mikroskopische Welt zu gewinnen.
Hat dich der Artikel Wellenlängen in der Fluoreszenzmikroskopie interessiert? Schau auch in die Kategorie Ogólny rein – dort findest du mehr ähnliche Inhalte!

