Die Parkinson-Krankheit, auch bekannt als idiopathisches Parkinsonsyndrom, ist eine komplexe neurologische Erkrankung, die das Leben der Betroffenen tiefgreifend beeinflusst. Ihre Geschichte ist eine Reise von der ersten Beschreibung der Symptome bis hin zu modernen, hochentwickelten Behandlungsmethoden. Doch trotz bedeutender Fortschritte in den letzten Jahrzehnten bleibt die Ursache der Krankheit bis heute unbekannt, und eine Heilung ist noch nicht in Sicht. Dieser Artikel beleuchtet die Entwicklung des Verständnisses und der Behandlung von Parkinson, die Vielfalt seiner Symptome von den ersten Anzeichen bis zu späten Stadien sowie die heute verfügbaren Therapieansätze.
Die offizielle Geschichte des idiopathischen Parkinsonsyndroms beginnt im Jahr 1817. Damals veröffentlichte der englische Arzt und Apotheker James Parkinson (1755–1824) in London seinen wegweisenden «Essay on the Shaking Palsy» (Abhandlung über die Schüttellähmung). Parkinson, ein vielseitig begabter Mann, der auch als Geologe und Paläontologe Bekanntheit erlangte, beschrieb darin erstmals detailliert die Kernsymptome der Erkrankung, die später seinen Namen tragen sollte. Seine Beschreibung umfasste unwillkürliche, zitternde Bewegungen (Tremor), eine verminderte Muskelkraft (Akinese), eine Neigung zu vornübergebeugter Körperhaltung und Schwierigkeiten beim Übergang von Gehen zu schnellerem Laufen. Bemerkenswerterweise stellte er fest, dass die Sinne und der Intellekt der Betroffenen unbeeinflusst blieben – eine wichtige Beobachtung, die sich allerdings nicht für alle Patienten und Stadien der Krankheit als zutreffend erweisen sollte. Trotz seiner präzisen Beschreibung der Symptome machte Parkinson in seinem Essay kaum therapeutische Empfehlungen. Er vertrat die Ansicht, dass eine medikamentöse Behandlung erst dann sinnvoll sei, wenn die Ursache der Krankheit besser verstanden würde.
Die Jahre nach James Parkinson waren geprägt von langsamen Fortschritten. Ein wichtiger Meilenstein in der sogenannten Vor-L-Dopa-Ära wurde rund vier Jahrzehnte später durch den französischen Neurologen Jean-Martin Charcot (1825–1893) gesetzt. Charcot, der an der berühmten Salpêtrière in Paris wirkte, fügte der Symptombeschreibung von Parkinson wichtige Details hinzu. Gemeinsam mit Alfred Vulpian beschrieb er erstmals den Rigor, die Muskelsteifheit, die heute zu den Kardinalsymptomen zählt und von Parkinson nicht explizit erwähnt wurde. Charcot prägte auch das Eponym «Maladie de Parkinson» und beschrieb weitere Symptome wie das Maskengesicht, den Verlust der Mimik. Seine Beobachtung, dass sich der Zustand mancher Patienten nach Bahn- oder Kutschenfahrten verbesserte, führte zur Entwicklung kurioser Therapieversuche wie eines Rüttelstuhls oder eines Rüttelhelms, in der Annahme, das Schütteln könne die Symptome lindern. Diese Methoden gerieten schnell in Vergessenheit. Nachhaltiger war die Entdeckung in Charcots Schule, dass das Belladonna-Alkaloid Hyoscin eine günstige Wirkung auf die Symptomatik hatte. Damit stand erstmals ein Medikament zur Verfügung, das die Symptome etwas lindern konnte. Anticholinergisch wirkende Substanzen blieben fast 100 Jahre lang die einzigen Medikamente mit klinisch relevantem Effekt auf Parkinson-Symptome. Auch heute noch werden sie, insbesondere zur Tremorbehandlung, eingesetzt, allerdings zurückhaltender aufgrund ihrer psychischen Nebenwirkungen.
Neben der medikamentösen Therapie gab es seit Ende des 19. Jahrhunderts auch chirurgische Versuche. Diese zielten oft darauf ab, Nervenbahnen zu durchtrennen, um den Tremor zu unterdrücken. Erst in den 1950er-Jahren berichteten Rolf Hassler und Traugott Riechert über gute Ergebnisse mit stereotaktischen Läsionen im Thalamus (Thalamotomie). Diese Methode, die den Tremor auf der Gegenseite unterdrücken und den Rigor mindern konnte, wurde weit verbreitet, hatte aber keinen Einfluss auf die Akinese. Bis zur Einführung von L-Dopa wurden weltweit viele solcher Eingriffe durchgeführt.
Der entscheidende Durchbruch in der Behandlung gelang mit der L-Dopa-Ära. Initiiert wurde diese durch den Wiener Pharmakologen Oleh Hornykiewicz. Zusammen mit H. Ehringer publizierte Hornykiewicz 1960 den bahnbrechenden Befund, dass in bestimmten Hirnregionen (Nucleus caudatus und Putamen) verstorbener Parkinsonpatienten ein stark verminderter Dopamingehalt vorlag. Diese Entdeckung fügte sich perfekt zu den Ergebnissen des schwedischen Pharmakologen Arvid Carlsson, der 1958 gezeigt hatte, dass ein künstlich ausgelöster Dopaminmangel bei Tieren Parkinson-ähnliche Symptome hervorrufen konnte, die durch Dopamingabe reversibel waren. Gleichzeitig wurde klar, dass Dopamin eine eigenständige Überträgersubstanz im Nervensystem ist und nicht nur ein Vorläufer von Noradrenalin und Adrenalin. Ein Problem war jedoch, dass Dopamin die Blut-Hirn-Schranke nicht überwinden konnte.
Hornykiewicz hatte die zündende Idee: Er erinnerte sich an die Arbeiten des Schweizer Chemikers Markus Guggenheim, der bereits 1913 L-Dopa, die Vorläufersubstanz von Dopamin, in Pflanzen nachgewiesen und ein Syntheseverfahren entwickelt hatte. Guggenheim konnte keine klinische Anwendung finden, aber Hornykiewicz vermutete, dass L-Dopa im Gegensatz zu Dopamin die Blut-Hirn-Schranke passieren und im Gehirn zu Dopamin umgewandelt werden könnte. Er überzeugte den Wiener Neurologen Walther Birkmayer, L-Dopa an Patienten zu testen. Im Sommer 1961 behandelte Birkmayer 20 Patienten intravenös mit kleinen Dosen L-Dopa. Die Ergebnisse waren spektakulär: Eine deutliche Besserung der Akinese trat ein und hielt über Stunden an. Birkmayer dokumentierte dies sogar in Filmen und wurde zu einem unermüdlichen Verfechter der Methode. Trotz positiver Ergebnisse anderer Forscher, wie André Barbeau, reagierte die Fachwelt zunächst skeptisch, teils ablehnend, da Doppelblindversuche fehlten. Der wissenschaftliche Durchbruch gelang erst um 1967, als George Constantin Cotzias in New York viel höhere, oral verabreichte Dosen von L-Dopa einsetzte, was zu überzeugenden Resultaten führte.
In der Schweiz kam L-Dopa 1970 als Larodopa® auf den Markt. Anfangs wurden sehr hohe Dosen verabreicht, was oft zu Übelkeit und Erbrechen führte. Dennoch war die Einführung von L-Dopa ein revolutionärer Fortschritt. Der Neurologe Oliver Sacks beschrieb in seinem Buch «Awakenings» (1973) eindrücklich, wie zuvor schwerstkranke Patienten durch L-Dopa zu neuem Leben erwachten. Es war eine euphorische Zeit, auch wenn die Erwartungen damals übertrieben waren – man hoffte sogar auf eine Heilung oder zumindest ein Stoppen des Fortschreitens der Krankheit.

Ein weiterer wichtiger Schritt war die Einführung der Decarboxylasehemmer Benserazid und Carbidopa. Die Idee dahinter war paradox: Man wollte L-Dopa zusammen mit einem Hemmer verabreichen, um zu sehen, ob die Wirkung ausbleibt. Doch das Gegenteil geschah: Die Wirkung wurde stärker. Der Grund: Decarboxylasehemmer können die Blut-Hirn-Schranke nicht passieren. Sie verhindern den vorzeitigen Abbau von L-Dopa zu Dopamin in der Peripherie, bevor es das Gehirn erreicht. So gelangt mehr L-Dopa ins Gehirn, und die Wirkung ist bei gleicher Dosis stärker. Dies ermöglichte eine Reduzierung der L-Dopa-Dosis um bis zu 90% und eine drastische Verringerung der Nebenwirkungen wie Übelkeit oder Herzrhythmusstörungen. 1973 kamen die Kombinationspräparate Madopar® (Benserazid-L-Dopa) und Sinemet® (Carbidopa-L-Dopa) auf den Markt. Damit stand erstmals eine wirklich wirksame und gut verträgliche Behandlung zur Verfügung. Allerdings zeigten sich bald Probleme der Langzeittherapie, wie unwillkürliche Bewegungen (Dyskinesien), Wirkungsschwankungen (Fluktuationen) und psychische Nebenwirkungen. Trotzdem ist die Kombination von L-Dopa mit einem Decarboxylasehemmer bis heute der Goldstandard der Parkinsontherapie.
Über die L-Dopa-Therapie hinaus wurden weitere Medikamente entwickelt. MAO-B-Hemmer (Rasagilin, Selegilin) sollten den Dopaminabbau im Gehirn verlangsamen, zeigten aber nur geringe klinische Verbesserungen. Eine neuroprotektive Wirkung wurde diskutiert, aber nicht zweifelsfrei bewiesen. Substanzielle Optimierungen brachten COMT-Hemmer (Tolcapon, Entacapon), die den peripheren Abbau von L-Dopa minimieren und dessen Bioverfügbarkeit verbessern, wodurch die Wirkung der einzelnen L-Dopa-Dosen verlängert wird. Amantadin, ursprünglich ein Grippemittel, wurde 1969 entdeckt und zeigte eine schwächere, aber nachweisliche Wirkung, insbesondere bei der Reduktion von Dyskinesien und Fluktuationen.
Eine sehr wichtige Entwicklung begann 1974 mit den ersten klinischen Studien zu Dopaminagonisten. Diese Substanzen (z.B. Bromokriptin, Rotigotin, Ropinirol, Pramipexol) stimulieren im Gehirn ähnliche Rezeptoren wie Dopamin. Als Monotherapie oft weniger wirksam als L-Dopa, zeigte sich, dass Patienten, die frühzeitig mit Dopaminagonisten behandelt werden, seltener und später Dyskinesien und Fluktuationen entwickeln. Neuere, nicht-ergoline Dopaminagonisten haben sich hierbei als erste Wahl etabliert, da ergoline Agonisten das Risiko von Herzklappenfibrosen bergen können.
Parallel zur medikamentösen Entwicklung wurden auch operative Methoden weiterentwickelt. Die stereotaktische Thalamotomie erlebte nach einem Rückgang durch L-Dopa eine Renaissance. Fortschritte in der Bildgebung ermöglichten präzisere Zielpunkte. Zudem wurden neue Zielpunkte im Gehirn gewählt, wie das Pallidum und der Nucleus subthalamicus, die nicht nur Tremor, sondern auch Rigor, Akinese und Dyskinesien günstig beeinflussen können. Die Pallidotomie wurde bereits 1952 von Lars Leksell durchgeführt, geriet aber in Vergessenheit, bevor sie in den 1990ern wieder aufgegriffen wurde.
Eine der bedeutendsten invasiven Behandlungsmethoden ist die Tiefe Hirnstimulation (THS), auch Hirnschrittmacher genannt. Pioniere wie Alim Benabid und Jean Siegfried zeigten, dass elektrische Stimulation den Tremor lindern kann. Anstelle destruierender Eingriffe werden heute zunehmend Elektroden implantiert, die mit einem Neuro-Schrittmacher verbunden sind. THS kann Symptome deutlich lindern und die Lebensqualität über Jahre stabilisieren, insbesondere bei Patienten mit Fluktuationen und Dyskinesien. Weitere invasive Verfahren sind die kontinuierliche Medikamentenabgabe mittels Pumpen, z.B. die Apomorphin- oder L-Dopa-Pumpe (Duodopa®), die ebenfalls eine verbesserte Symptomkontrolle ermöglichen.
Neben diesen medizinischen und chirurgischen Behandlungen sind nicht-medikamentöse Therapien von entscheidender Bedeutung für die Lebensqualität der Patienten. Dazu gehören Physiotherapie zur Verbesserung von Bewegung und Gleichgewicht, Ergotherapie zur Erhaltung der Selbstständigkeit im Alltag und Logopädie zur Behandlung von Sprach- und Schluckstörungen. Diese Therapien helfen, körperliche Fähigkeiten zu erhalten und den Alltag zu bewältigen.
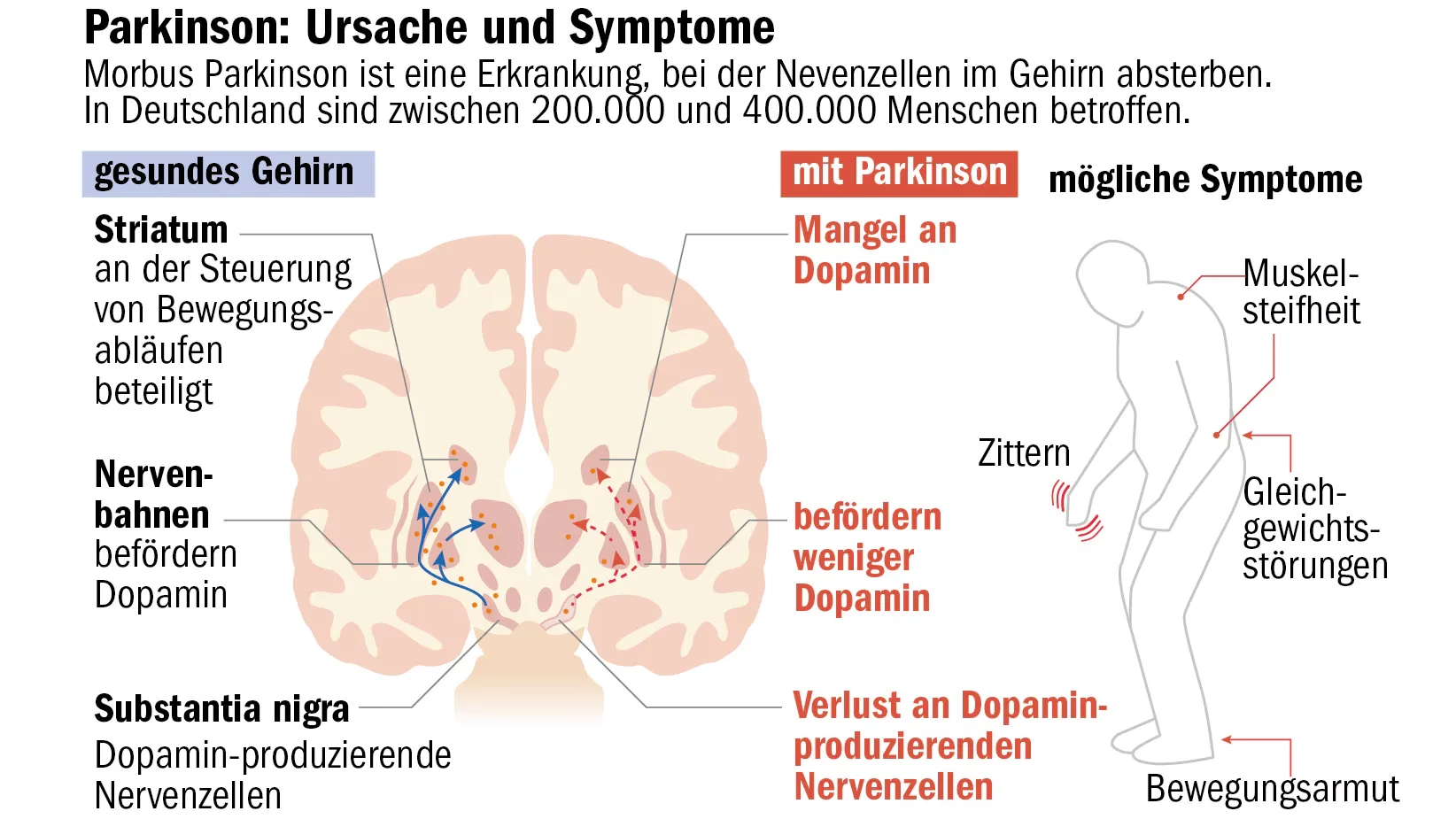
Das Fortschreiten der Parkinson-Symptome ist von Person zu Person sehr unterschiedlich. Wann, wo und wie stark Symptome auftreten, variiert stark. Frühe Anzeichen sind oft unspezifisch und betreffen weniger die Motorik. Dazu zählen Störungen des Geruchssinns, Tagesmüdigkeit, REM-Schlaf-Verhaltensstörungen, Verstopfung, Sehstörungen, Reizbarkeit, Antriebslosigkeit und Depressivität. Auch Veränderungen bei Mimik, Stimme und Sprache (leiser, höher, zittrig, langsamer oder beschleunigt) können erste Hinweise sein. Chronische Verspannungen und unspezifische Muskel-/Gelenkschmerzen sind ebenfalls möglich. Motorische Frühsymptome treten oft einseitig und schwach auf: ein Arm schwingt beim Gehen nicht richtig mit, leichte Feinmotorikprobleme (Schuhe binden, Tippen), leicht schlurfender Gang, kleinere Schritte, leichte Ruhe-Tremor in einer Hand (Pillendreher-Tremor), veränderte Handschrift. Deutlich sichtbare motorische Symptome wie gebeugte Körperhaltung oder langsames Gehen zeigen sich meist erst später, wenn bereits ein Großteil der dopaminproduzierenden Zellen abgestorben ist. Man spricht dann von den Kardinalsymptomen: Akinese (Bewegungsarmut/-verlangsamung), Rigor (Muskelsteifheit) und Tremor (Zittern).
Im Spätstadium treten motorische Symptome beidseitig auf und nehmen an Intensität zu. Der Ruhe-Tremor kann sich auf Arme, Beine, Füße oder Kopf ausbreiten. Gangunsicherheit mit kleinen Schritten, erhöhte Sturzgefahr durch gestörte Reflexe, deutliche Verlangsamung und Blockaden (Freezing) erschweren Bewegungen. Schluckstörungen und Darmträgheit nehmen zu. Das Maskengesicht wird ausgeprägter, Stimme und Sprache verändern sich stark. Im Spätstadium können kognitive Dysfunktionen bis hin zur Parkinson-Demenz auftreten. Eine seltene, aber schwere Komplikation ist die akinetische Krise, ein Zustand vollständiger Bewegungsunfähigkeit. Die Intensität der Symptome kann im Tagesverlauf schwanken, beeinflusst durch Medikamentenspiegel, psychische Faktoren wie Angst oder Stress sowie Begleiterkrankungen wie Infektionen.
Es ist wichtig zu wissen, dass Parkinson selbst keine lebensbedrohliche Krankheit ist. Mit der heutigen Behandlung, bestehend aus Medikamenten (oft L-Dopa in Kombination mit Decarboxylasehemmern, Dopaminagonisten, COMT-Hemmern, MAO-B-Hemmern, Amantadin, Anticholinergika), invasiven Verfahren wie THS oder Pumpen und nicht-medikamentösen Therapien, kann die Lebensqualität und Eigenständigkeit oft bis ins hohe Alter weitgehend erhalten werden. Allerdings erfordert das Leben mit Parkinson, insbesondere im fortgeschrittenen Stadium, oft einen hohen Energieeinsatz, da viele Handlungsabläufe bewusst gesteuert werden müssen und nicht mehr automatisch erfolgen. Fatigue, eine Begleiterkrankung, die zu körperlicher, seelischer und kognitiver Erschöpfung führt, ist ebenfalls eine Herausforderung.
Parkinson kann weitere Erkrankungen wie Depressionen, Angststörungen und Demenz nach sich ziehen. Spezialisierte Neurologen erkennen diese Begleiterkrankungen frühzeitig und können entsprechende Behandlungen einleiten, oft durch eine Kombination aus Medikamenten (z.B. Antidepressiva) und Psychotherapie.
Behandlungsmöglichkeiten im Überblick
Die Therapie von Parkinson hat sich über zwei Jahrhunderte dramatisch entwickelt. Heute stehen verschiedene Ansätze zur Verfügung, die oft kombiniert eingesetzt werden:
| Therapieprinzip | Wirkstoffe/Methoden | Wirkmechanismus | Vorteile | Nachteile/Hinweise |
|---|---|---|---|---|
| Dopaminersatz | L-Dopa (oft mit Decarboxylasehemmern: Madopar®, Sinemet®) | Wird im Gehirn zu Dopamin umgewandelt, ersetzt fehlenden Botenstoff | Stärkste Wirkung auf motorische Kernsymptome (Akinese, Rigor, Tremor) | Kurze Halbwertszeit, Wirkungsschwankungen, Dyskinesien bei Langzeitgebrauch, anfängliche Übelkeit/Erbrechen möglich |
| Dopaminrezeptorstimulation | Dopaminagonisten (z.B. Rotigotin, Ropinirol, Pramipexol) | Stimulieren Dopaminrezeptoren direkt | Längere Wirkdauer, potenziell weniger Dyskinesien bei Therapiebeginn, transdermales Pflaster möglich (Rotigotin) | Häufigere nicht-motorische Nebenwirkungen (Wassereinlagerungen, Schläfrigkeit, Verstopfung, Übelkeit), weniger wirksam als L-Dopa bei fortgeschrittener Krankheit |
| Dopaminabbauhemmung | MAO-B-Hemmer (Rasagilin, Selegilin) | Hemmen den Abbau von Dopamin im Gehirn | Leichte symptomatische Wirkung, potenzielle neuroprotektive Wirkung (nicht gesichert) | Geringere Wirksamkeit als L-Dopa/Agonisten |
| L-Dopa-Bioverfügbarkeitsverbesserung | COMT-Hemmer (Tolcapon, Entacapon) | Hemmen den peripheren Abbau von L-Dopa | Verlängerung der L-Dopa-Wirkdauer, Reduktion von Off-Phasen | Werden nur in Kombination mit L-Dopa gegeben, spezifische Nebenwirkungen möglich |
| Andere Medikamente | Amantadin, Anticholinergika | Verschiedene Mechanismen (z.B. Amantadin bei Dyskinesien, Anticholinergika bei Tremor) | Gezielte Wirkung auf bestimmte Symptome | Nebenwirkungen (z.B. psychische Effekte bei Anticholinergika) |
| Invasive Verfahren | Tiefe Hirnstimulation (THS), Pumpentherapien (Apomorphin, L-Dopa) | Elektrische Stimulation bestimmter Hirnregionen (THS), kontinuierliche Medikamentenzufuhr | Deutliche Linderung von Fluktuationen/Dyskinesien (THS), stabile Symptomkontrolle (Pumpen), Verbesserung der Lebensqualität in fortgeschrittenen Stadien | Chirurgischer Eingriff erforderlich (Infektionsrisiko, Angst vor OP), nicht für alle Patienten geeignet, THS wirkt nicht auf alle Symptome gleich gut |
| Nicht-medikamentöse Therapien | Physiotherapie, Ergotherapie, Logopädie | Übungen zur Verbesserung von Bewegung, Alltagskompetenz, Sprache, Schlucken | Erhalt/Verbesserung körperlicher Fähigkeiten, Steigerung der Lebensqualität, keine Medikamenten-Nebenwirkungen | Erfordert Eigeninitiative und regelmäßiges Training |
Häufig gestellte Fragen zu Parkinson
Wann wurde Parkinson entdeckt?
Die Krankheit wurde erstmals 1817 von dem englischen Arzt James Parkinson in seinem «Essay on the Shaking Palsy» detailliert beschrieben.
Wie hat sich die Behandlung von Parkinson entwickelt?
Nach ersten zaghaften Ansätzen mit Substanzen wie Hyoscin und chirurgischen Versuchen in der Vor-L-Dopa-Ära, revolutionierte die Einführung von L-Dopa in den 1960er Jahren die Therapie. Später folgten Kombinationspräparate mit Decarboxylasehemmern, Dopaminagonisten, MAO-B- und COMT-Hemmer. Seit den 1990er Jahren spielen auch invasive Methoden wie die Tiefe Hirnstimulation und Pumpentherapien eine wichtige Rolle. Nicht-medikamentöse Therapien sind ebenfalls essenziell.
Was sind die wichtigsten Symptome von Parkinson?
Die sogenannten Kardinalsymptome sind Akinese (Bewegungsarmut/-verlangsamung), Rigor (Muskelsteifheit) und Tremor (Zittern im Ruhezustand). Im Frühstadium können unspezifische Symptome wie Geruchsstörungen, Schlafprobleme, Verstopfung, Müdigkeit oder depressive Verstimmungen auftreten. Später entwickeln sich sichtbare motorische Probleme wie Gangunsicherheit, Gleichgewichtsstörungen, gebeugte Haltung und Schwierigkeiten bei Feinmotorik.
Gibt es eine Heilung für Parkinson?
Nein, eine Heilung für die Parkinson-Krankheit ist bisher nicht möglich. Alle verfügbaren Therapien zielen darauf ab, die Symptome zu lindern und das Fortschreiten der Krankheit zu verlangsamen bzw. die Lebensqualität zu erhalten. Die Ursache der Krankheit ist noch unbekannt, was eine kausale Behandlung erschwert.
Wie wird Parkinson diagnostiziert?
Die Diagnose von Parkinson basiert in erster Linie auf der ärztlichen Beurteilung der typischen klinischen Symptome, insbesondere der motorischen Kardinalsymptome wie Akinese, Rigor und Tremor, die im fortgeschrittenen Stadium eindeutiger in Erscheinung treten. Frühsymptome sind oft unspezifisch und machen eine Diagnose im Anfangsstadium schwierig. Weitere diagnostische Verfahren können unterstützend eingesetzt werden, aber die klinische Untersuchung ist entscheidend.
Wie lange lebt man noch nach der Diagnose Parkinson?
Die Parkinson-Krankheit selbst ist in der Regel keine direkt lebensbedrohliche Erkrankung. Mit den heutigen Behandlungsmöglichkeiten kann die Lebensqualität und Eigenständigkeit oft viele Jahre, teilweise bis ins hohe Alter, aufrechterhalten werden. Die Lebenserwartung kann durch die Krankheit beeinflusst werden, aber nicht so stark wie früher. Spätkomplikationen wie schwere Schluckstörungen, Stürze oder eine Parkinson-Demenz können jedoch die Lebenserwartung und -qualität beeinträchtigen.
Wo stehen wir heute? Seit den 1960er-Jahren hat die Forschung und Behandlung von Parkinson rasante Fortschritte gemacht. Während in den ersten 150 Jahren seit James Parkinsons Beschreibung nur kleine Schritte erzielt wurden, haben die Entdeckung von L-Dopa und die Entwicklung weiterer Medikamente sowie invasiver Therapien das Leben vieler Betroffener erheblich verbessert. Zielgerichtete Therapien und neue Forschungsansätze im Bereich der Gentherapie und Neuroimmunologie sind vielversprechend, befinden sich aber noch in der klinischen Prüfung.
Zusammenfassend lässt sich sagen, dass die Hoffnung von James Parkinson, bald ein Mittel gegen Parkinson zu finden, das die Krankheit aufhält oder heilt, bis heute unerfüllt geblieben ist. Die Ursachen bleiben im Verborgenen. Dennoch haben die intensiven weltweiten Bemühungen zu Therapien geführt, die das Leiden der Betroffenen signifikant lindern und ihre Lebensqualität verbessern. Die Geschichte der Parkinson-Behandlung ist eine Geschichte des Fortschritts im Kampf gegen eine der komplexesten neurologischen Erkrankungen, und die Forschung nach neuen, noch effektiveren Therapien und hoffentlich einer Heilung geht weiter.
Hat dich der Artikel Parkinson: Geschichte, Symptome & Therapie interessiert? Schau auch in die Kategorie Ogólny rein – dort findest du mehr ähnliche Inhalte!
